クマリン類とフェナジン類の化学生態がPseudomonads の鉄獲得に及ぼす影響
クマリン類とフェナジン類の化学生態がPseudomonads の鉄獲得に及ぼす影響
The chemical ecology of coumarins and phenazines affects iron acquisition by pseudomonads
Darcy L. McRose, Jinyang Li, and Dianne K. Newman
PNAS  2023  Vol. 120  No. 14  e2217951120
(要旨)
二次代謝産物は、根圏における植物-微生物相互作用の重要な促進因子であり、コミュニケーション、競争、栄養獲得に寄与している。
しかし、一見したところ、根圏には重複した機能を持つ代謝産物があふれているように見え、代謝産物の利用を支配する基本原理についての理解は限られている。
必須栄養素である鉄へのアクセスを増加させることは、植物と微生物の酸化還元活性代謝物(RAM)の両方が果たす重要な役割の一つであるが、一見冗長に見える。
我々は、モデル植物であるシロイヌナズナが作るRAMであるクマリンと、土壌に生息するシュードモナドが作るRAMであるフェナジンを用いて、植物と微生物のRAMがそれぞれ異なる環境条件下で異なる機能を持つかどうかを調べた。
その結果、酸素とpHの変化により、クマリン類とフェナジン類の鉄制限性仮種細菌の増殖能に予測できる違いが生じること、また、これらの効果は、仮種細菌をグルコース、コハク酸、ピルビン酸のいずれで増殖させるかによって異なることが明らかになった。この結果は、これらの代謝産物の化学反応性と、微生物代謝によって変化するフェナジン類の酸化還元状態によって説明される。
この研究結果は、化学的な微小環境の変化が二次代謝産物の機能に大きな影響を与えることを示しており、植物が根の滲出液中に放出される炭素を変化させることで、微生物の二次代謝産物の有用性を調整できる可能性を示唆している。
これらの知見を総合すると、RAMの多様性は、化学生態学のレンズを通して見ると、それほど圧倒されるものではないことが示唆される: 異なる分子は、それらが存在する局所的な化学的微小環境に応じて、鉄の獲得など特定の生態系機能にとってより重要であったり、重要でなかったりすることが予想される。
(まえがき)
二次代謝産物は、根圏における植物-微生物および微生物-微生物の相互作用を制御する役割を果たすとして、その評価が高まっている。
しかし、根圏 には、一見化学的に冗長な性質を持つ植物や微生物の代謝産物が数多く存在する。このことはパラドックスを提示している。もしこれらの分子が実際には冗長であるなら、なぜこれほど多くの分子が存在するのだろうか?
その答えのひとつは、機能的な冗長性を評価する我々の能力が、それらが占めるさまざまな化学的ニッチについての不完全な理解によって制限されているからである。
ほとんどの微生物系を特徴づける急峻な化学的勾配を考慮すると、時間と空間におけるダイナミックな化学的変化が、微生物の反応性に制約を与えているのではないかと推測したくなる。
二次代謝産物の反応性に制約を与え、二次代謝産物により微妙な機能と高い特異性を付与しているのではないかと推測したくなる。言い換えれば 化学生態学の枠組みが、この明白なパラドックスを説明する助けになるかもしれない。
この考えを検証するには特異性が必要であるため、我々は必須金属である鉄(Fe)と土壌生態系におけるその役割に注目した。鉄へのアクセスを増加させることは、土壌二次代謝産物の重要な役割のひとつであるが、まだ十分に解明されていない。
酸素の多い環境では、鉄はしばしば 鉄(III)-オキシ水酸化物として沈殿することが多いが、これは比較的利用しにくい。植物は、鉄の生物学的利用能 を高めるために、いくつかの戦略を開発してきた: 鉄 シデロフォアやフィトシデロフォアのような鉄(III)結合分子の生成、鉄(III)の酸化還元活性代謝産物(RAM)によるFe(III)からFe(II)への還元、根圏の酸性化などである。
シデロフォアとRAMの生産は細菌に広く見られ、多くの生物が両方の代謝物を生産している。二次代謝産物の生産は 真性イネ科植物はフィトシデロフォアを生産する傾向があるが、RAM生産は他のすべての植物に利用されている。
シデロフォアは、特殊な分子機構を介してのみ鉄と複合体を形成し、鉄へのアクセスを制御することによって、微生物の競争を促進する可能性があることが以前から認識されていた。合成微生物群集を用いた最近の研究から、異なるシデロフォア生産者の存在が、根圏微生物群集を形成し、植物病原菌の抑制と増殖の両方に寄与することが示されている。
土壌微生物群集における鉄の利用可能性の調節におけるRAMの役割については、シデロフォアよりもはるかにわかっていない。
RAMとシデロフォアは、植物または微生物の代謝物のどちらかに焦点を当ててきた。しかし RAMが土壌の鉄循環において重要な役割を果たしていることを示す証拠は多い。
また、RAMの化学的特性は、化学的条件の変化に特に敏感であるため、異なる環境条件下では、異なるRAMがより有用であったり、より有用でなかったりすることを示唆している。
テストケースとして、我々は植物のクマリンと細菌のフェナジン類に焦点を当てた。
クマリンは、モデル植物のシロイヌナズナ(Arabidopsis thaliana)を含む多くの植物で作られ、鉄制限下での植物の成長に重要である。
根圏細菌に対するクマリンの影響を探る研究は、その毒性(主に活性酸素種、ROSの生成による)と根のマイクロバイオームの特定のメンバーを抑制する能力に焦点を当てている。クマリンの鉄制限土壌細菌に対する潜在的な増殖効果や、これらの細菌が作る内因性代謝産物との相互作用については、ほとんど未解明である。
フェナジン類は、そのような細菌産生RAMのひとつであり、クマリンと同様に活性酸素を発生させることで抗生物質としての性質を持つが、鉄の可溶化にも役立つ。
フェナジン類は土壌に生息する数多くの細菌によって生産され、その中でも最もよく研究されている生産者であるシュードモナドでは、フェナジン類がバイオフィルム形成を促進するのに必要な過剰量の鉄を遊離することが示されている。
一見似ているように見えるが、クマリンとフェナジンの反応性の違いから、これらの代謝物が異なる条件下で鉄の可溶化に有用である可能性が示唆される(図1)。
RAMは、代謝産物から鉄(III)への電子移動を通じて鉄を遊離する。つまり、RAMは還元された電子運搬状態でのみ鉄を可溶化することができる。還元型フェナジンは酸素との反応性が高く、しばしばO2をO2-に還元する。
対照的に、還元型クマリンは酸素との反応性が低いようである。さらに フェナジンはシュードモナドによって(再)還元される。還元力は炭素源の形で、このプロセスに不可欠である。
フェナジン還元における炭素源の重要性は、植物の根からの滲出物が重要な炭素源である根圏において特に興味深く、滲出液の変化が二次代謝産物の有用性を変える可能性がある。
我々は、酸素、pH、炭素源の変動がRAMの酸化還元状態を変化させ、フェナジンとは対照的にクマリンの化学的ニッチ フェナジン類とは対照的に、クマリン類には異なる化学的ニッチが形成されるという仮説を立てた。
我々の第一の目的は 二次代謝産物は、鉄の可溶化という具体的な事例を中心としているが、その局所的な 化学的コンテクストを考慮することで、二次代謝産物をより良く理解できるかもしれないという、より広範な考えを探ることである。
クマリンとフェナジン類の化学的特性解析と、様々な酸素濃度、様々なpHで培養したシュードモナドの増殖実験を通して、この考えを検証した。
また、根の滲出液に含まれるコハク酸、グルコース、ピルビン酸を炭素源とする培養実験も行った。
我々の結果は、根圏におけるRAMによる鉄可溶化の化学生態学に光を当て、根滲出液が微生物の二次代謝産物の有用性を調整する、というこれまで知られていなかったメカニズムを示唆している。
(実験方法と結果は省略)
(結論)
我々の研究は、化学的に異なる酸化還元活性を持つ土壌二次代謝物
二次代謝産物は、様々な酸素 pH、および炭素のレジームが変化すると、鉄の獲得に関して異なる機能を発揮することを示した。
我々の研究から予想されることは、よりアルカリ性で水はけのよい(つまり酸化的な)土壌ではRAMに基づく鉄の可溶化には、フェナジンよりもクマリンの方が重要である。
さらに一般的には、二次代謝産物の冗長性というパラドックスは、その化学的生態学的ニッチを時空間的に高解像度で考慮することで解決できる可能性があることを、原理的に証明した。
より一般的には、我々の発見は、二次代謝産物の冗長性のパラドックスが、その化学生態学的ニッチを高い時空間分解能で考慮することによって、部分的に解決される可能性があることを原理的に証明するものである。
しかしながら、バルク土壌や母材に見られる化学的パラメータが、植物の根で経験される微小環境においてどの程度維持されているのかについては、完全には理解されていない。
実際に、植物による炭素の放出と微生物による酸素の消費を通じて、植物と微生物の代謝の相互作用が、化学的な微小環境と二次代謝産物の生物学的影響に大きな影響を与える可能性があることが示された。
今後の大きな課題は、その場の根圏条件が空間的・時間的にどのように変化するかを明らかにすることである。
図1. 根圏酸化還元活性代謝物(RAM)の化学生態学は、一見冗長に見えるその機能を解明するのに役立つかもしれない。
(A)植物のクマリン(緑色) とバクテリアのフェナジン(オレンジ)は、どちらも鉄の可溶化を助けるRAMである。しかし、環境化学的な変化によって、一方の代謝産物が他方の代謝産物に有利に働くかどうかは不明である。
代謝産物間の顕著な違いの1つは、フェナジン類はクマリン類よりも酸素との反応性が高いことである。
( B)クマリンとフェナジンでは、酸素とpHの変動によって定義されるレジームにおいて、クマリンとフェナジンの方が鉄の獲得を促進する効果が高いという、明確な化学的生態学的ニッチを予測することができる。
フェナジン類(オレンジ色)は、微生物によって還元されやすい環境で最も有用である。すなわち、低pH、低酸素、還元性炭素源の存在下である。
クマリン類(緑色)は、酸素との反応性が低く、微生物による還元を必要としない。クマリン(緑)は、酸素との反応性が低く、鉄を遊離させるために微生物による還元を必要としないため、幅広い環境条件下で有用となる可能性がある。
(Cox):炭素の酸化状態。
図2. クマリンとフェナジンPCAの化学的性質。
(A)pH5.5、6.5、7.5におけるダフネチン、フラキセチン、PCAの可逆的酸化還元活性を示すボルタンモグラム。5.5、6.5、7.5で測定した。
実験は、酸素雰囲気下(クマリン)または窒素雰囲気下(PCA)で1 mMの代謝物を用いて行った。
スコポレチンのCVプロファイルは複雑である。クマリンのCV(cyclic voltammetry)実験では金の作用電極を用い、PCAのCV実験ではグラッシーカーボンの作用電極を用いた。
クマリンとPCAの電位の大きな違いに注意。
(B) 酸素存在下(黒)または非存在下(青)における、異なる代謝物による鉄還元。
実験は、FeCl3として40μMのFe(III)と20μMの各代謝物を用いてpH7.5で行われ、Fe(II)はフェロジンアッセイで検出され、2:1の代謝物を示した: Fe(II)の化学量論が示された。
重複アッセイは2つの別々の線で示した。
(C)酸化および還元クマリンとPCAの構造。
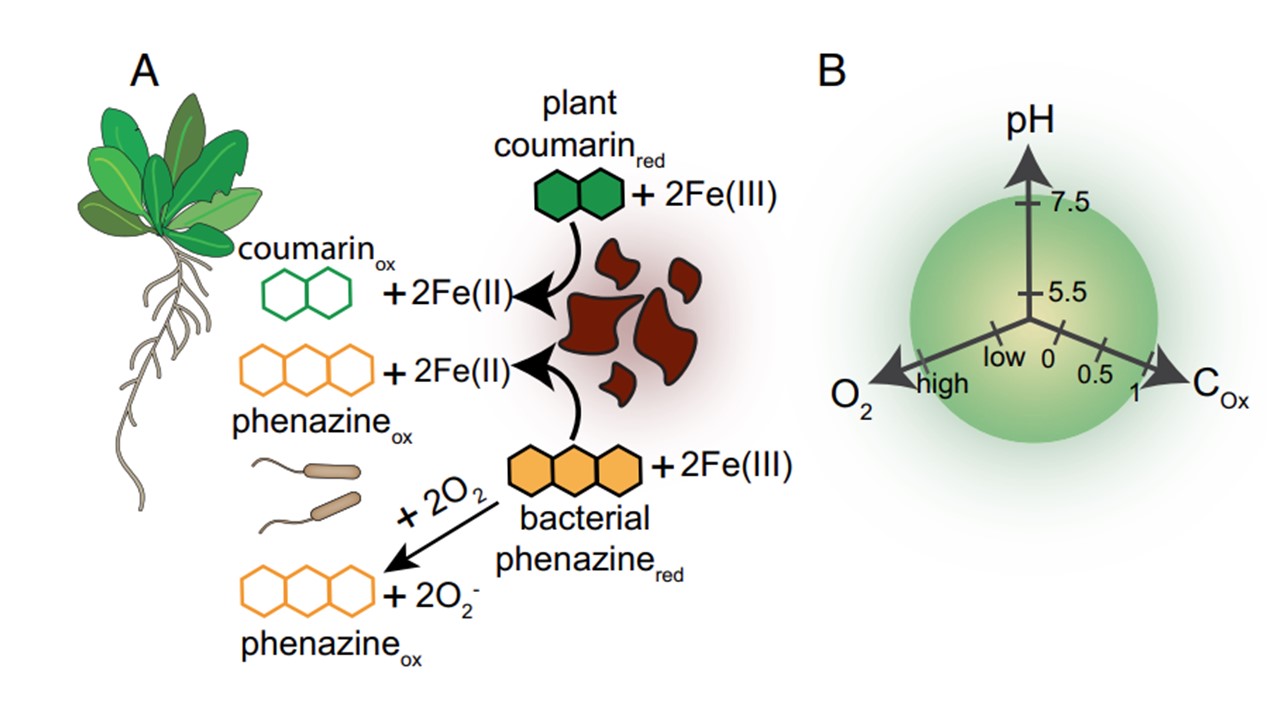
図1
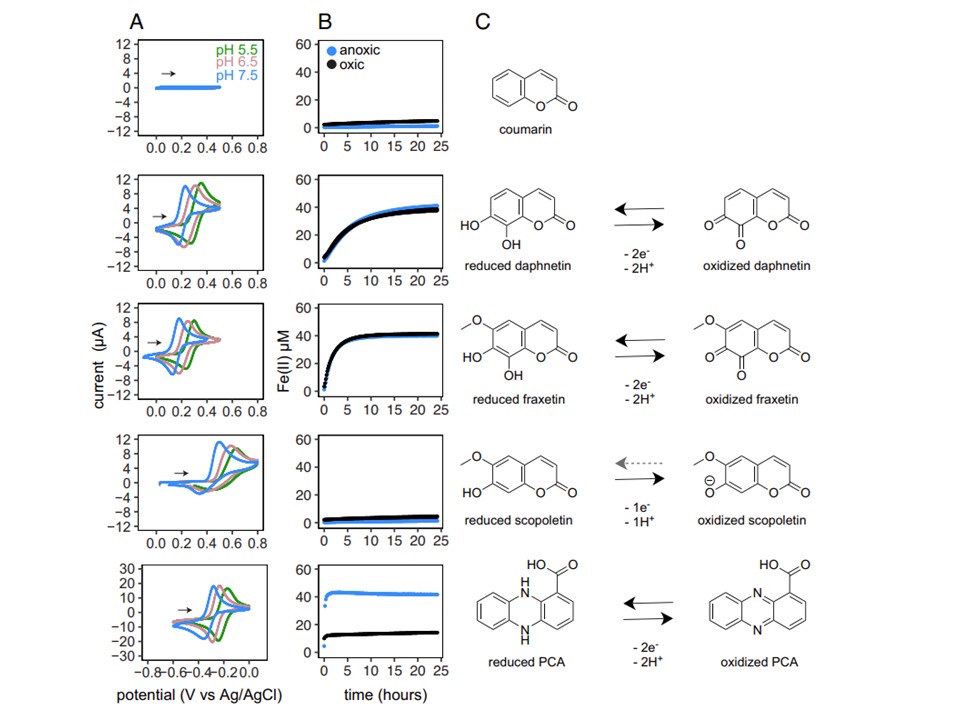
図2