イネの亜鉛吸収におけるフィトシデロフォアの作用機序の解明:地球化学的勾配と正確な安定定数の重要性
イネの根圏環境によってイネがIRT1でZn2+で吸収するのか、YSLを経由してZnDMAで吸収するのかは、詳細な研究がなされていない。この論文では根圏環境を変化させた場合のZn吸収のシミュレーションを計算機科学の手法で行ったものである。鈴木基史君のZn関連論文が頻回に引用されている。
イネの亜鉛吸収におけるフィトシデロフォアの作用機序の解明:地球化学的勾配と正確な安定定数の重要性
Unravelling the modus operandi of phytosiderophores during
zinc uptake in rice: the importance of geochemical gradients
and accurate stability constants
George H.R. Northover, Enrique Garcia-Espana and Dominik J. Weiss
Journal of Experimental Botany, Vol. 72, No. 5 pp. 1517–1526, 2021
(これまでのZn吸収研究の総括)
亜鉛吸収におけるファイトシデロフォアの機能理解のための重要な進展
- イネにおけるファイトシデロフォアによる亜鉛の取り込みの同位体証拠
Markovicら(2017)は、Zn(II)-DMA錯体におけるZnの同位体標識が、野外実験で栽培したイネの茎におけるZnの同位体標識(Arnoldら、2010)と一致することを実験的に実証した(A)。
次のステップは、イネがZnを取り込む際のDMAの作用機序を理解することである。
- 根圏におけるシデロフォアと他のリガンドとの相乗効果的な役割
McRoseら(2018)は、自然溶液中に共存するリガンドの生態系に注目している。
彼らは、バクテリアのシデロフォアを介した鉄取り込みの汎用モデルを提案しており、シデロフォア(高親和性Y)は低親和性リガンド(X)と相乗的に働くことが示唆されている(B)。
このことから、Zn(II)-DMAの根圏での安定性は、土壌中に存在する他の金属やリガンド(有機物・無機物)との競合的相互作用に依存することが示唆された。
- 金属の生物学的利用能における地球化学的勾配の重要な役割。
Liuら(2020)は、地球化学的スペシエーション・モデリングを用いて、バルク水中と比較して境界層に見られる異なるpHと酸素濃度を考慮すると、2価および3価の金属の藻類吸収に関する予測が大幅に改善されることを実証した(C)。
この研究により、根圏に存在する地球化学的勾配が微量栄養素の取り込みプロセスに与える影響を考察することができる(Vetterlein and Jahn, 2004; Raynaud, 2010; Gao et al.)
- 金属-シデロフォア複合体の安定性定数を計算で決定した。
Kirbyら(2020)は、電子構造計算が、シデロフォア官能基を持つ金属の親和定数を高速かつ正確に決定する方法を提供することを立証している。このアプローチは、シデロフォアリガンドサンプルの調達の課題を回避する方法を提供するものである。
(本研究の概要)
微量栄養素の欠乏は、世界の食糧生産に脅威を与えている。
稲の亜鉛欠乏は深刻な問題である。
亜鉛が土壌からイネに移行する経路の一つとして、ファイトシデロフォアの一つであるデオキシムギニン酸(DMA)が提案されている。
イネ科植物の栄養学において、フィトシデロフォアが鉄以外の広い役割を担っているという考えはよく知られている。
しかし、イネにおけるDMAを介した亜鉛の取り込み経路の詳細については、まだ不明な点が多く残されている。
特に、DMAから亜鉛がどのような形で取り込まれるのか(遊離のZn(II)またはZn(II)-DMA錯体として)、また他の金属とDMAの競合挙動がどのような役割を果たすのかが問題である。
我々は、pH、配位子濃度、イオン性の変化の影響を正確に記述することを提案する。
イオン強度の変化がZn(II)-DMA錯体の安定性に及ぼす影響を正確に説明することが、亜鉛の取り込みにおけるDMAの作用機序を理解する上で重要であることを提案する。
そのため、根細胞周辺の微小環境における地球化学的変化の重要性を明らかにし、不正確な安定定数がスペシエーションモデルに与える影響を実証した。
(はじめに)
作物植物における微量栄養素の欠乏は、世界の食料安全保障に大きなリスクをもたらす(Oliver and Gregory, 2015; Elliott, 2017)。
その結果、バイオフォート化に向けた作業を支援することが急務となっている。すなわち、選択的な育種、遺伝子、環境工学技術を通じて作物の栄養密度含有量を増加させるプロセスである(Nestel et al.、2006年)。
バイオフォート化の成功は、微量金属のホメオスタシスと、土壌から穀物への金属の移動に関わる段階を詳細に理解することにかかっている。
イネ(Oryza sativa)における亜鉛欠乏は、世界の食糧安全保障の中核をなす重要な栄養問題であり、世界の低地イネの総収量の最大50%に影響を及ぼしている(Muthayya et al,2013).
イネの遺伝子発現研究および滲出液プロファイリング調査から得られた証拠は、内因性デオキシムギネ酸(DMA; Suzuki et al.、2008)の濃度の増加、および根細胞から周辺環境へのDMAの高い流出速度と亜鉛欠乏に対する耐性向上とを関連付けた(Suzuki et al.、 2008; Widodo et al.、2010)。
DMAはフィトシデロフォアの一種で、イネ科植物が生産する低分子有機化合物の一つであり、鉄(III)に高い親和性を持っている。
DMAの根細胞からの放出はイネの亜鉛効率に関係することが知られているが、DMAによるイネの亜鉛吸収の機構モデルには重要な知見が不足している。
これらは、予測的な取り込みモデルの開発を妨げ、解離しないZn(II)-DMA複合体が取り込まれるかどうかなどの重要な疑問に答える能力を低下させている。
(結論)
(i) イネの亜鉛効率におけるDMAの重要性とそのメカニズムを議論する上で、根細胞周囲の微小環境における地球化学的変化の影響が重要であることを示した。
溶液化学の正しい理解に基づくモデリングを用いて、DMAの選択性を評価・検討する必要がある。
(ii)根圏における金属-DMA錯体の安定場を特定するための不正確な安定定数の影響を示す。
純粋な配位子サンプルの入手の問題や、根圏で重要な金属や配位子の数が多いことを考慮し、電子構造計算を利用して正確な安定定数を決定できることを提案する。
(iii) 正確なスペシエーションモデルを作成するためには、pHと[L]に次いで、安定定数のイオン依存性を決定する必要があることを示す。
このためには、複数のイオン強度でKconditionalを決定する必要がある。既製のモデリングコードで使われている単純な活性係数のアプローチでは不十分である。
Fig1 の説明
(a)中性状態のDMA(C12H20N2O7)のボールアンドスティックダイアグラム。
aはこれらの部位の酸解離定数(pKa)が表示されている。赤、白、灰、青はそれぞれ、酸素、水素、炭素、窒素を表す。
bは関連分子である乳酸のアルコール性プロトンのpKaに基づく推定値(Silvaら、2009)。
(b)イネ科植物および植物プランクトンにおけるリガンドアシストによる取り込みの研究に基づいて、イネにおけるZn(II)-DMA錯体からの亜鉛の取り込みに関する3つの戦略を提案した(Von Wiren et al, 1996; Aristilde et al., 2012):
(1) Zn(II)は吸収される前に根の細胞表面から離れた位置でDMAからアンロードされる。
(2)非解離型 Zn(II)-DMA 複合体は,根の細胞表面から吸収される前に,根の細胞表面から離れた場所に輸送される。
DMA複合体は、推定上の細胞膜輸送体を介して膜を越えて輸送される。
(3)根の細胞表面でZn(II)が一過性の三元錯体を形成してDMAから剥離し、(1)と同様にリガンドなしで内在化する。
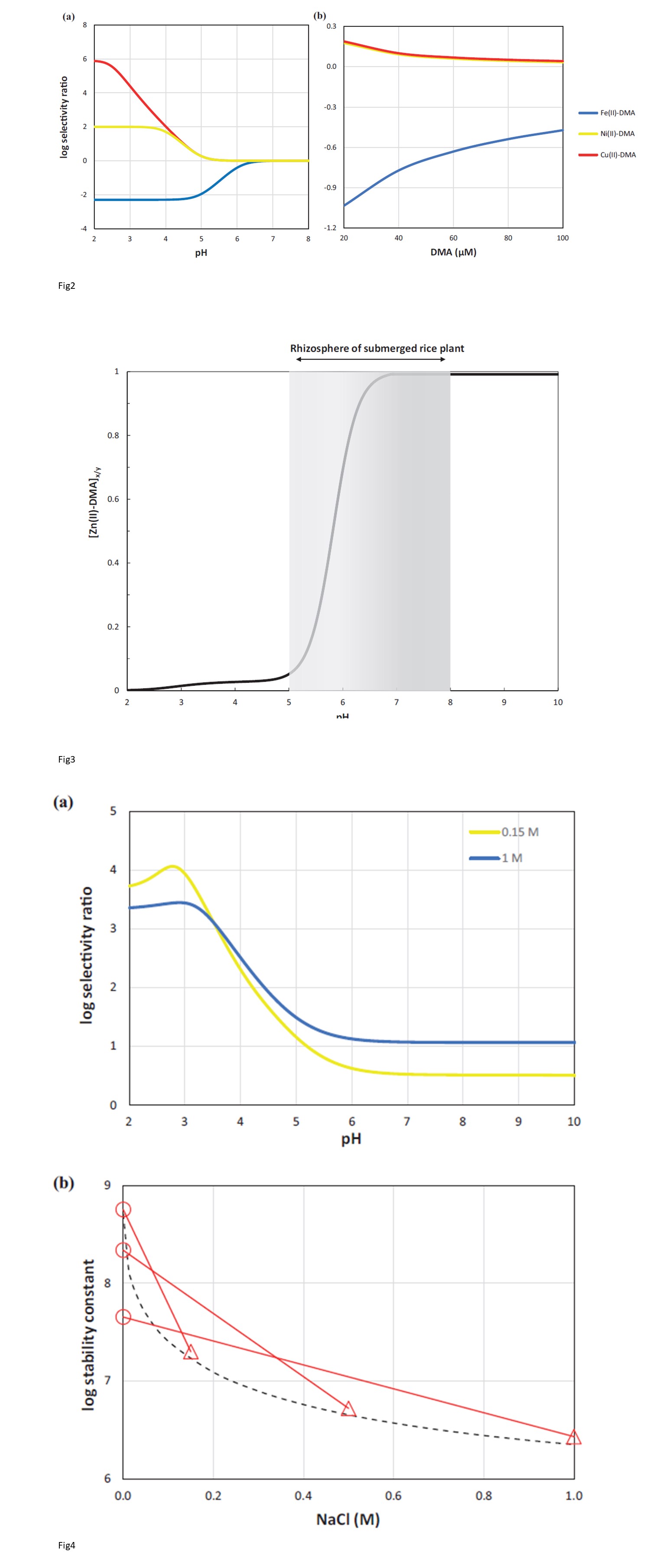
Fig2.の説明
DMA の Zn(II)に対する選択性を他の金属と比較し、(A) pH と (B) DMA 濃度の関数として、選択性比を用いて表現した。
(log S, M/M); S=[M-DMA]/[Zn(II)-DMA]. 全ての系で[M]=1μM、[Zn(II)]=1μMである。(A)では[DMA]=10μM、(B)はpH5.5である。モデリングを行った。
村上ら(1989)が決定した安定定数を用いてモデル化した。
Fig3.の説明
2つの同一の系 [Fe(II)=1 μM, Zn(II)=1 μM, DMA=10 μM] における Zn(II)-DMA 濃度の比率を、2つの異なるセットの安定性を用いてモデル化したものである。
安定定数、x=Murakamiら(1989); Fe(II)=10.1, Zn(II)=12.7; y=Sugiuraら(1981); Fe(II)=8.1, Zn(II)=10.7 を用いてモデル化した。
[Zn(II)-DMA]x/y<1、濃度 村上ら(1989)系のZn(II)-DMAの濃度が、杉浦ら(1981)系のZn(II)-DMAの濃度より低いことを示す。
[Zn(II)-DMA]x/y>1である。
村上ら(1989)系のZn(II)-DMAの濃度は、杉浦ら(1981)系のZn(II)-DMAの濃度より大きい。
灰色の は、水中土壌におけるイネの根圏のpHの範囲を示す。
Fig4. の説明
(A)2つの同一の系{[Zn(II)]=1 μM, [Sn(II)]=μM, [クエン酸]=10 μM}におけるZn(II)対Sn(II)のクエン酸の選択性、イオン強度は2種類で
S=[Sn(II)-citrate]/[Zn(II)-citrate] の選択比(log S, M/M)で表される。
モデリングは、Cigalaら(2013, 2015)によって決定された安定定数を利用して実施した。
(B)赤色は、Zn(II)-PO4について実験的に決定された3つのKconditional値を三角形で示した(Cigala et al.、2012a)。
活性係数を計算するためにDavies方程式を使用して決定されたこれらの点のK固有値を赤丸で示す。
黒丸は、3つのZn-PO4 Kconditional値を用いて、Extended Debye-Huckel方程式の修正版をパラメータ化したものである。
このモデル は破線で示されている。
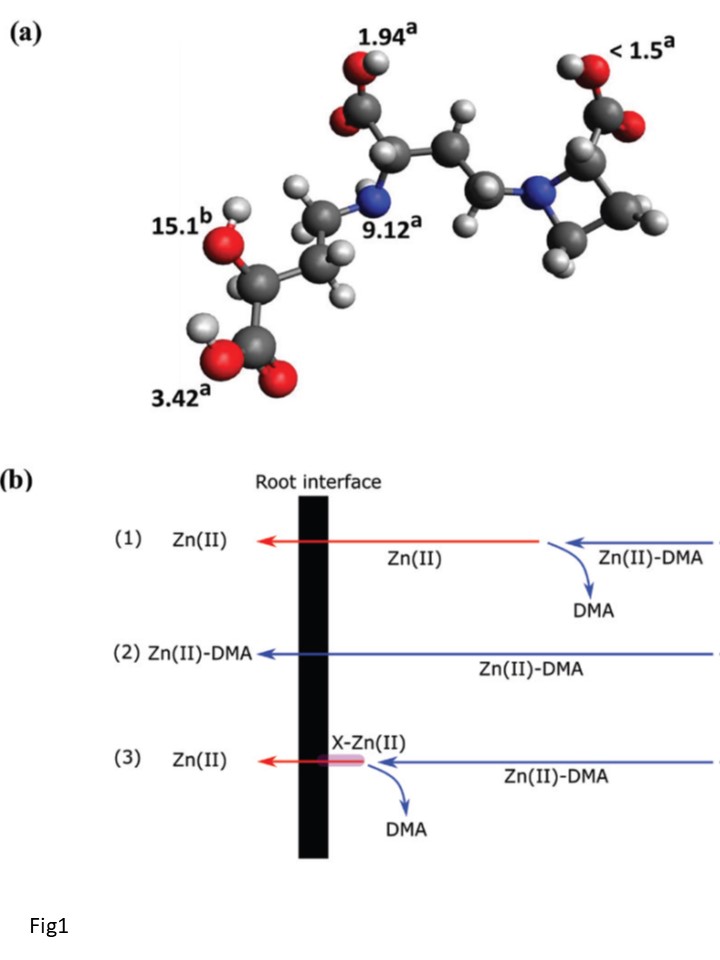
Fig1
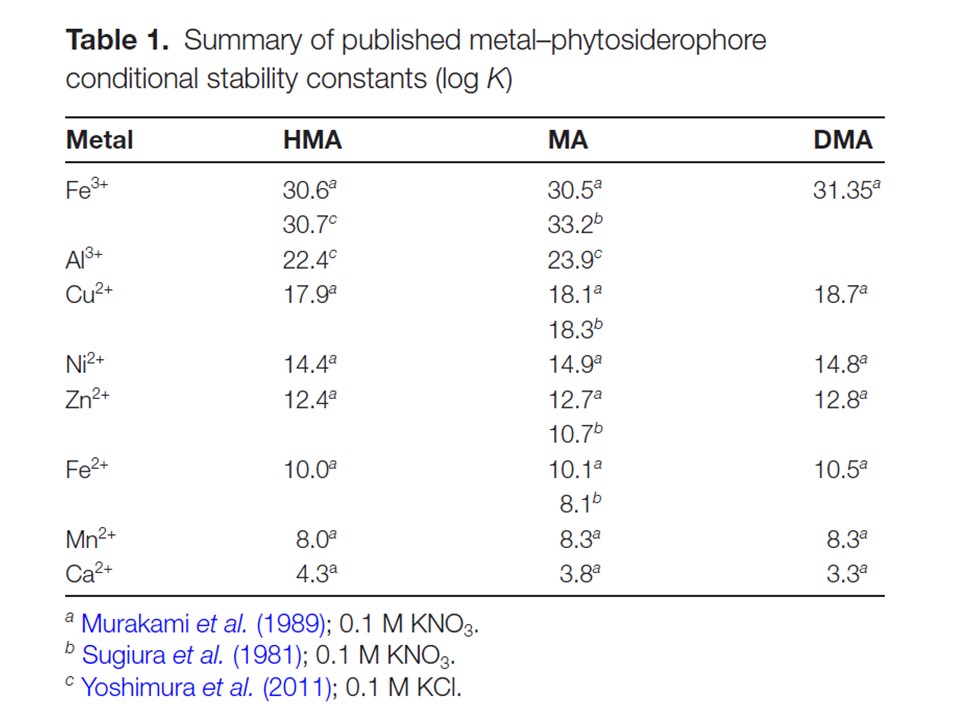
Table1
F1g2,Fig3,Fig4